ライフテクノロジーズジャパン株式会社 バイオサイエンス事業部
- HOME
- ライフテクノロジーズジャパン株式会社 バイオサイエンス事業部
- 製品・サービス詳細
- トランスフェクションが困難な細胞のためのエレクトロポレーター ― Neon NxT Electroporation System
会社カテゴリー:研究関連資材
主サービス提供地域:
製品・サービス詳細
トランスフェクションが困難な細胞のためのエレクトロポレーター ― Neon NxT Electroporation System
サービスカテゴリー:モダリティ、再生医療、分析、研究・開発
トランスフェクションが困難な細胞のためのエレクトロポレーター
Neon NxT Electroporation System
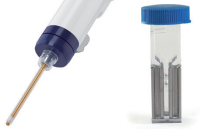
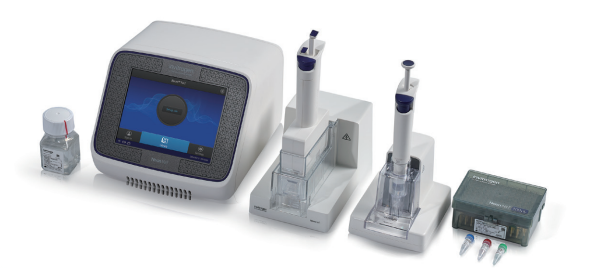
Invitrogen™ Neon™ NxT Electroporation Systemは、哺乳類細胞のトランスフェクションワークフローを合理化する革新的な設計を備えた次世代のエレクトロポレーションプラットフォームです。生物学的に適合したピペットチップとバッファーチューブに配置した電極により、これまでのエレクトロポレーションデバイスより均一な電界が作られるため、トランスフェクション効率や細胞生存率が大幅に向上します。
Invitrogen™ Neon™ NxTピペットチップはトランスフェクションチャンバーとしての役目も果たすため、一般的なエレクトロポレーターのようにキュベットへのサンプルの出し入れやキャップの着脱の必要はありません。エレクトロポレーション後はNeon NxTピペットチップからサンプルが直接培地へ排出されます。ピペット操作手順が減るため、サンプルのロスを最小限に抑え、細胞が受けるせん断力を減らし、サンプルの汚染リスクを減らすことが可能です。このようなNeon NxT Electroporation Systemが持つシンプルなエレクトロポレーションワークフローにより、取り扱いが難しい細胞株でも安心してトランスフェクションが可能です。
Neon NxT Electroporation Systemのメリット
実証済みの性能と卓越した細胞生存率 ― 当社独自のエレクトロポレーションチップテクノロジーにより、困難な細胞株でも確実にトランスフェクションし、細胞生存率を維持します。
サンプルの保護 ― 独自のNeon NxTピペットチップにより、エレクトロポレーション用キュベットやプレートを別途用意する必要がありません。装置のコンパクトな設計により、バイオセーフティキャビネット(BSC)内に簡単に設置することができます。サンプルの移動で貴重な細胞が失われることはなく、汚染されるリスクも減らせます。
時間の短縮 ― 単一のバッファーキットを使用して、3つの簡単なステップで細胞をトランスフェクションします。操作はNeon NxTピペットチップに細胞やペイロードを吸引し、ピペットステーションにセットして[Electroporate]を押すだけです。これだけでトランスフェクションされた細胞を培養容器に移す準備が整います。
Invitrogen™ Neon™ NxT 8チャンネルピペットおよびプレートフォーマットであれば、96サンプルを15分以内にトランスフェクションできます。
フレキシビリティ ― さまざまな細胞タイプ、細胞密度、ペイロードおよび用途に対応するエレクトロポレーションパラメーターを詳細に最適化できます。エレクトロポレーション1回あたり2 × 104個~6 × 106個の細胞をトランスフェクションします。
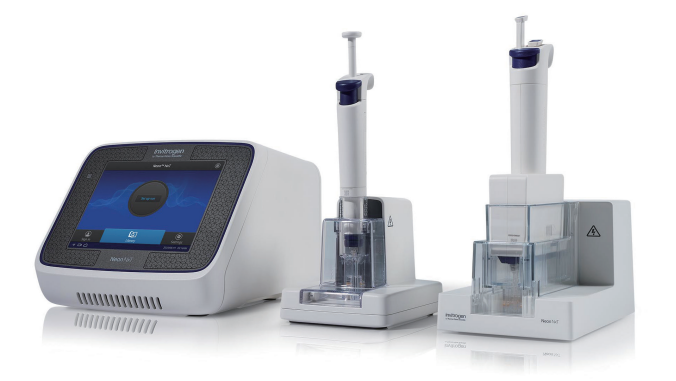
実証済みのトランスフェクション効率
当社独自のエレクトロポレーションチップテクノロジーにより、高い細胞生存率を保ちながら、導入困難な哺乳類細胞を効率的にトランスフェクションできます。免疫細胞、初代細胞、幹細胞などの非常に難易度の高い細胞においても、非常に優れたトランスフェクション効率と細胞生存率(図1)が得られています。
トランスフェクション後の優れた細胞生存率
私たちは、お客さまの細胞がどれほど大切かを理解しています。そのためNeon NxT Electroporation Systemは、より制御された状況下でのエレクトロポレーションの実現と2回のピペッティング工程を削減します。エレクトロポレーションを行うために別のキュベットにピペットで出し入れする必要がないので、細
胞が受けるせん断力も少なくなります。これらの特長により、増殖やトランスフェクションが困難な細胞を取り扱う場合に特に重要な細胞死を最小限に抑えられます(図1)。
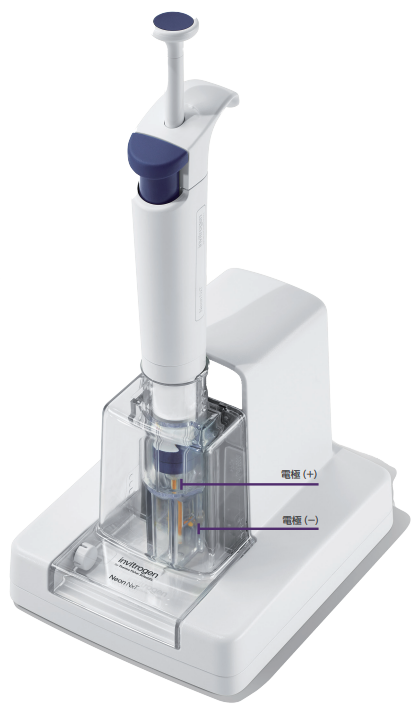
Neon NxT Electroporation System内の電極は互いに離れて配置されているため、表面面積が最も少なくなります。ディスポーザブルのNeon NxTピペットチップに一方の電極を配置し、他方の電極はInvitrogen™ Neon™ NxTバッファーチューブの下部に配置されます。表面面積が少ないため、pH変化が最小限でより均一な電界が生成されます。エレクトロポレーション中に生成される熱やイオンも低減されるので、生理的状態が大きく阻害されません。
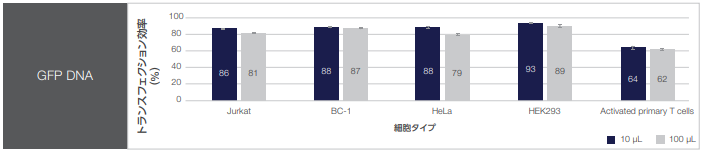
トランスフェクション効率
細胞生存率
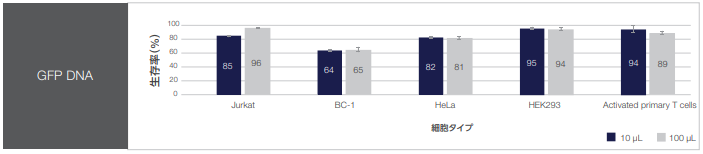
図1. Neon NxT Electroporation Systemを使用した際のトランスフェクション効率およびトランスフェクション後の細胞生存率。
細胞は10 μLまたは100 μLのエレクトロポレーション反応において、GFPプラスミドDNAでトランスフェクションしました。トランスフェクション効率はGFP陽性細胞(n = 3)の割合を示します。トランスフェクションされた細胞はInvitrogen™ SYTOX™ Red Dead Cell Stainで染色し、 Invitrogen™ Attune™ NxT Flow1 Cytometerで生存率を評価しました。細胞生存率(%)は、3回の測定の平均値を示します。
 当社のエレクトロポレーションチップテクノロジーは14,000件を 当社のエレクトロポレーションチップテクノロジーは14,000件を超えるピアレビュージャーナルで引用されています。 |
|
Neon NxT Electroporation Systemは以下により高い細胞生存率を可能にします
|
 |
 Neon NxT Electroporation Systemは、アーク放電や過剰なエネルギーパルスの照射を防止するためのエネルギー計算機能を備えています。 Neon NxT Electroporation Systemは、アーク放電や過剰なエネルギーパルスの照射を防止するためのエネルギー計算機能を備えています。また、アーク検出機能を内蔵しており、処理に失敗したサンプルを特定することができます。 |
貴重なサンプルを保護
サンプルの移動ロスを最小限に
サンプルは貴重であるにもかかわらず、従来のキュベットタイプでの移し替えでは多少のロスは避けられませんでした。
Neon NxT Electroporation Systemでのエレクトロポレーションは、キュベットではなくピペットチップ内部で行われるため、サンプルのロスや細胞が受けるせん断力を最小限に抑えることができます。
サンプルの汚染を最小限に
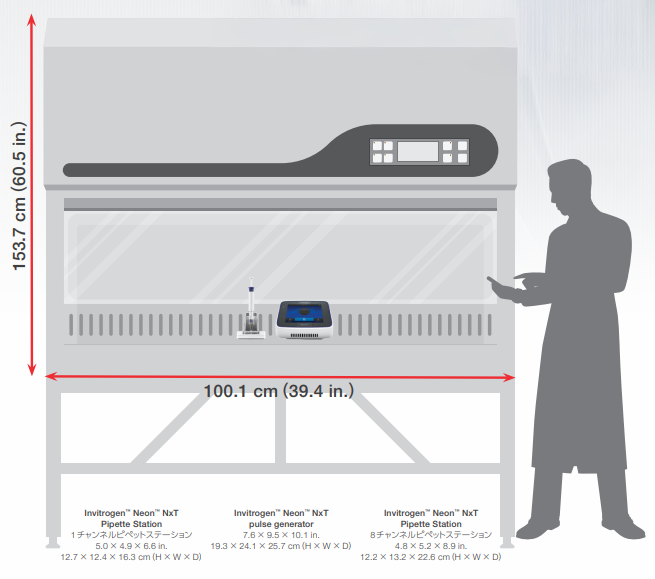
Neon NxT Electroporation Systemはパルスジェネレーターやピペットステーションを含みますが、設置面積が小さいため、ほとんどの BSC 内に収めることができます。そのため、機器使用中は常にサンプルが無菌エリア内部にとどまり、貴重な細胞が汚染されるリスクを減らせます。Neon NxT Electroporation Systemには、BSC内での使用を簡素化する新しいケーブル管理機能も備わっています。
 Neon NxT Electroporation Systemはコンパクトな設計のため、 Neon NxT Electroporation Systemはコンパクトな設計のため、サッシを上げることなくBSCから簡単に出し入れ可能です。 |
ゲノム編集の効率向上
ゲノム編集は、創薬プロセスの変革、疾患モデルの作成、細胞・遺伝子治療法の開発など、ヒトの健康と病気の理解を深めるために大きな期待が寄せられています。
ゲノム編集ワークフローにおいて重要でありながら困難なステップは、CRISPRリボヌクレオタンパク質(RNP)、DNA、RNA分子を、選択した細胞株に効率的に導入することです。上記のように、エレクトロポレーションは、トランスフェクションが困難な細胞でも高い効率を達成できるため、最も広く使用されている導入方法です。
当社のゲノム編集試薬および Invitrogen ™ Neon ™ NxT Resuspension Genome Editing Buffer を Neon NxT Electroporation Systemと併用することで、初代細胞、幹細胞、トランスフェクション困難な細胞などの哺乳類細胞を用いたノックアウトやノックイン実験でのCRISPR Cas9などの特定のペイロードを用いた、ゲノム編集性能を向上させることができます(図2)。
その他のデータについては、困難な細胞種で高いゲノム編集効率を達成するためのアプリケーションノートをご覧ください。
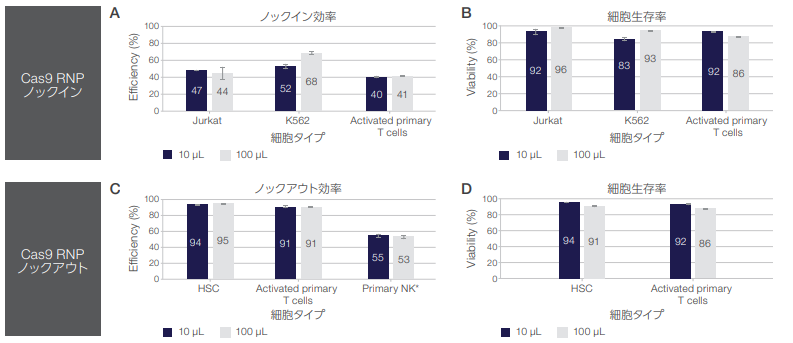
図2. さまざまな細胞種とターゲットにおけるCRISPR-Cas9に基づくゲノム編集実験でのNeon NxT Resuspension Genome Editing Bufferの性能。
標的遺伝子座には、Jurkat細胞およびK562細胞のACTN、活性化初代T細胞のTRAC、造血幹細胞のB2M、初代NK細胞のAAVS1が含まれます。細胞は10 μLまたは100 μLの反応でエレクトロポレーションされました。(A)GFPドナーDNAのノックイン効率は、GFP陽性細胞の割合を示します。(B)GFPドナーDNAノックイン後の細胞の生存率です。(C)ノックアウト効率は、未処理のコントロールと比較した、特定の標的遺伝子座の減少パーセントとして示します。(D)ノックアウト細胞の電気穿孔後の生存率です。
注意事項:初代NK細胞については、Invitrogen™ GeneArt™ Genomic Cleavage Detection (GCD)アッセイで求めたインデル効率(%)をノックアウト効率の代わりとして記載しています。
 Neon NxT Electroporation Systemのゲノム編集プロトコルは、Invitrogen™ TrueGuide™ Synthetic gRNAおよび Invitrogen™ TrueCut ™ Cas9 タンパク質を用いて最適化されています。 Neon NxT Electroporation Systemのゲノム編集プロトコルは、Invitrogen™ TrueGuide™ Synthetic gRNAおよび Invitrogen™ TrueCut ™ Cas9 タンパク質を用いて最適化されています。TrueCut Cas9タンパク質は、臨床およびトランスレーショナルアプリケーションにも利用可能で、あらゆる段階でお客さまのニーズをサポートします。 |
高いフレキシビリティ
|
カスタマイズ可能なパラメーター • パルス電圧 • 細胞タイプ |
 Neon NxT Electroporation Systemは、最大 10,000 個のプロトコルを保管できます。 Neon NxT Electroporation Systemは、最大 10,000 個のプロトコルを保管できます。 |
| さまざまなペイロード、細胞タイプ、および細胞密度に対応 1反応あたり2 × 104個~6 × 106個の細胞を柔軟にトランスフェクションでき、DNA、RNA、またはタンパク質を広範な哺乳類細胞に導入します。150 個を超えるエレクトロポレーションプロトコルと、細胞株、細胞タイプ、ペイロード、製品、および文書の種類(プロトコル、アプリケーションノート、論文)ごとにフィルタリングできる引用ライブラリーで、さまざまなトランスフェクションアプリケーションに対応します。 |
 Invitrogen™ TransfectionSelect™ ツールは、入力した条件に基づきプロトコルライブラリーをフィルタリングするので、アプリケーションに適したプロトコルを見つけられます。 Invitrogen™ TransfectionSelect™ ツールは、入力した条件に基づきプロトコルライブラリーをフィルタリングするので、アプリケーションに適したプロトコルを見つけられます。 |
|
1つのバッファーキットで多くの哺乳類細胞腫に対応可能
|
 GEバッファーは、R バッファーと比較してノックイン効率を最大5倍、向上させることができます。 GEバッファーは、R バッファーと比較してノックイン効率を最大5倍、向上させることができます。 |
研究時間を短縮
|
簡素化されたワークフロー 処理時間の短縮 Neon NxTエレクトロポレーションワークフロー
|
 |
 Thermo Scientific™ ClipTip™ テクノロジーにより、Neon NxTピペットチップは所定の位置に配置されるとカチッと音がします。 Thermo Scientific™ ClipTip™ テクノロジーにより、Neon NxTピペットチップは所定の位置に配置されるとカチッと音がします。チップ装着と排出に強い力は必要ないため人間工学的にもメリットがあります。 |
プレートのセットアップ時間を短縮
プレートセットアップモードが作業効率をレベルアップします。Neon NxT Electroporation Systemの直感的なユーザーインターフェースで、エレクトロポレーション実験のセットアップを効率的に行えます。クイックスタートを利用してサンプルごとにエレクトロポレーションパラメーターを調整する代わりに、プレート全体を事前にセットアップし、各サンプルをエレクトロポレーションする際に画面上で進捗をモニターできます。
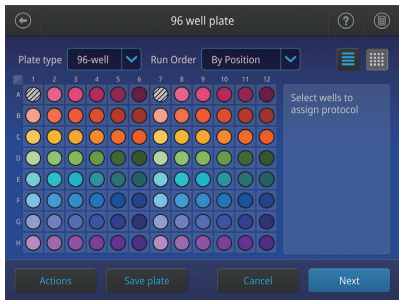
 Neon NxT 8チャンネルピペットを使用すると96サンプルを15分 Neon NxT 8チャンネルピペットを使用すると96サンプルを15分以内にエレクトロポレーションできます。 |
TransfectionLabアプリを使用してクラウドベースで簡単に計画立案
Thermo Fisher™ Connect Platformから入手できるInvitrogen™ TransfectionLab™アプリを使用することで、エレクトロポレーションパラメーターを最適化して生産性とトレーサビリティを向上できます。
実験の詳細を入力すると、設計ステージから実験に合わせたステップ・バイ・ステップガイドが作成されます
 最大 384 個のサンプルに対し複数のプレートレイアウトをリモートでセットアップできます。Neon NxT Electroporation Systemのユーザーインターフェースではなく、クラウドを介してアプリに保存された任意のプロトコルやプレートレイアウトにアクセスできます。 最大 384 個のサンプルに対し複数のプレートレイアウトをリモートでセットアップできます。Neon NxT Electroporation Systemのユーザーインターフェースではなく、クラウドを介してアプリに保存された任意のプロトコルやプレートレイアウトにアクセスできます。 |
8チャンネルピペット、パフォーマンスを維持しスループットを向上
Neon NxT 8チャンネルピペットは、柔軟性をかつてないレベルにまで高めました。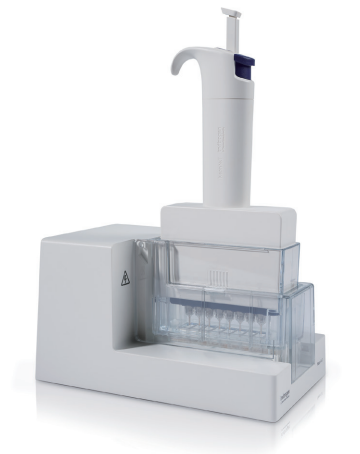
8チャンネルピペットの各チップは、独立したチューブ内で独立して動作するため、チップごとに異なるエレクトロポレーションパラメーター、再懸濁バッファー、デリバリーペイロード、あるいは細胞の種類を使用することができます。
さらに、Neon NxT 8チャンネルピペットとピペットステーションは、既存のNeon NxT Electroporation Systemと連動し、同じNeon NxTチップとバッファーを活用できます。条件を最適化する場合でも、複数の変数を探索する場合でも、Neon NxT 8チャンネル・ピペットは、研究を加速し、信頼性の高い結果を得るために必要な汎用性を提供します。
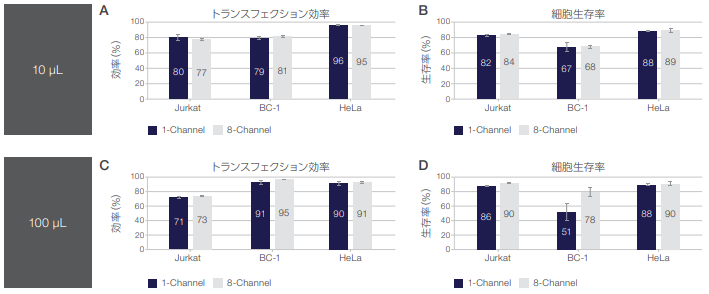
図3. Neon NxT 1チャンネル vs 8チャンネルピペット性能比較。
(A)10 μLでのトランスフェクション効率(%GFP細胞)です。(B)10 μLでのトランスフェクション後の細胞生存率です。(C)100 μLでのトランスフェクション効率(%GFP細胞)です。(D)100 μLでのトランスフェクション後の細胞生存率です。全てのグラフはn = 8で実施しました。
最適化を最大化する柔軟性
Neon NxT 8 チャンネルピペットは、各チャンネルを異なる条件に設定できるため、1回の実験で幅広いパラメーターを効率的にテストでき、研究のスループットと精度が大幅に向上します。図 4は、Jurkat細胞における11.5 kb GFP プラスミドトランスフェクションに最適なエレクトロポレーションプログラムと再懸濁バッファーを評価した結果です。
特定のエレクトロポレーションプログラムを表す各データポイントは、生存トランスフェクト細胞総数(TVTC)に対するエレクトロポレーション24 時間後の GFP 陽性細胞の割合を示しています。赤丸は、T バッファーで最大 85%のトランスフェクション効率を達成し、最も良好な条件を示しています。この合理的なアプローチにより、迅速かつ正確な最適化が可能になり、実験において高い効率と生存率を確保するのに役立ちます。
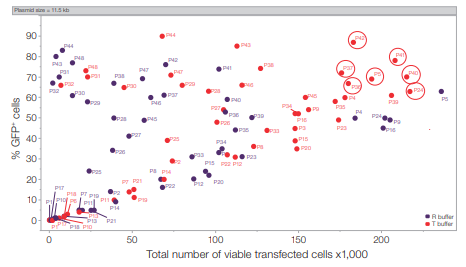
図4. 11.5kbのGFPプラスミドに対する48プログラムでのRバッファー vs Tバッファーのエレクトロポレーション性能。
GFP 陽性細胞の%をTVTCに対してプロットしました。グラフ中の各データ点(n = 1)は、特定のエレクトロポレーションプログラムを表します。グラフ中の赤丸は、最も成績のよい条件を示すデータ点を示しており、GFP陽性細胞の割合が高く、TVTCが高いという微妙なバランスが特長です。
バッファーの最適化でパフォーマンスを向上
アプリケーションごとに適したバッファーの選択は、最適なトランスフェクション効率と生存率の達成に極めて重要です。使用目的によりそれぞれ推奨の再懸濁バッファーが異なりますが、最適化を行うことにより、適切なバッファーを選択することができます。図 5に示されているように、活性化プライマリーT 細胞への CRISPR RNP導入は、GEバッファーで最もうまくいきます(A)。Jurkat 細胞では、R バッファーがより小さなプラスミドに適しており、Tバッファーがより大きなプラスミドに優れていることが分かります(C)。入念な最適化によってバッファーの選択を調整すれば、実験結果を大幅に向上させることが可能となります。
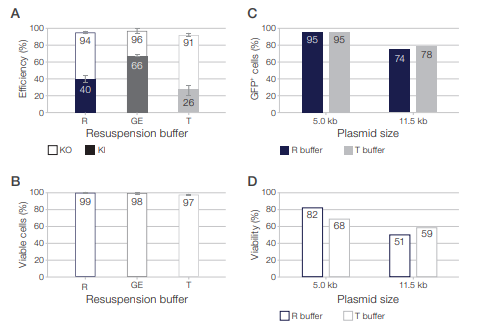
図 5. さまざまなアプリケーションにおける Neon NxT 再懸濁バッファーの評価。
(A)活性化プライマリーT 細胞における CRISPR/Cas9 を介したノックアウト/ノックイン(KO/KI)アプリケーションのための R、GEおよび Tバッファーを用いた編集効率の比較です。(B)R、GE、Tバッファーの対応する細胞生存率です。(C)サイズの異なるプラスミドをJurkat細胞に導入する際のRおよびTバッファーを用いたトランスフェクション効率の評価しました。(D)RおよびTバッファーの対応する細胞生存率です。
最適化プロセスをさらに加速
実験計画法(DOE)に対応した Neon NxT Electroporation Systemと8チャンネルピペットにより、研究者は複数の変数を同時に探索・最適化し、結果の信頼性と堅牢性を高めることができます。
DOEを活用することで、さまざまな要因間の相互依存関係を特定し、直接テストされていない最適条件を予測することができるため、包括的かつ効率的な最適化が可能になります。本システムは、DOEに基づく生物学的研究において、迅速かつ効果的なパラメーター・スクリーニングを可能にする卓越したシステムです。
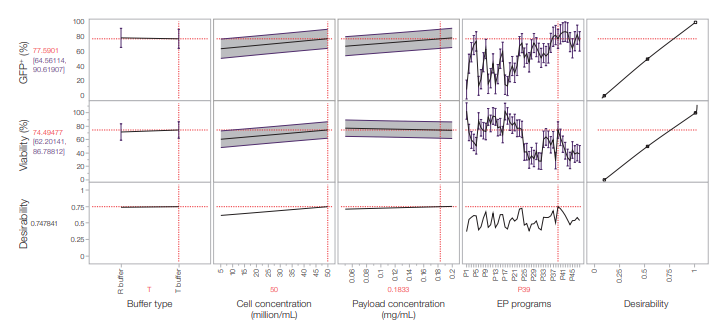
図6. JMPソフトウエアを利用したDOE予測プロット。
入力因子はx軸に表示され、y軸は予測された応答を表します。垂直の赤線は各要因の現在値を示し、因子の現在値は、横軸の下に赤くハイライトされています。縦軸の赤い値は、要因の現在値に基づいて予測された反応を表している。これらの現在値は、予測モデルによって、各応答の重要度が等しく、最大の望ましさを達成するための最適値として生成されたものです。
 オプションとして、Neon NxT Electroporation Systemのフィールドサービスエンジニアによる設置適格性評価と動作適格性評価 オプションとして、Neon NxT Electroporation Systemのフィールドサービスエンジニアによる設置適格性評価と動作適格性評価(IQOQ)をご用意しています。これによりお客さまの時間と労力を節約できます。 |
仕様

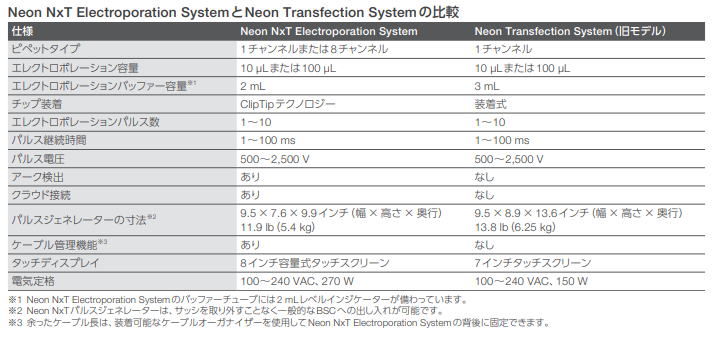
同一のテクノロジー、同一の性能
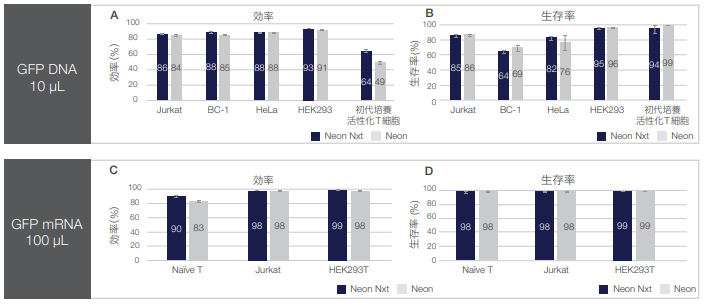
図7. Neon NxT Electroporation SystemとNeon Transfection Systemの性能。
性能は、さまざまな哺乳類細胞株をGFPプラスミドDNAまたはGFP mRNAとともにトランスフェクションして評価しました。(A)GFP陽性細胞の割合で示したGFPプラスミドDNAのトランスフェクション効率を示します。(B) GFPプラスミドDNAでのトランスフェクション後の細胞生存率です。(C)GFP陽性細胞の割合で示したGFP mRNAのトランスフェクション効率を示します。(D)GFP mRNAでのトランスフェクション後の細胞生存率です。
参考文献
1. Kim J-A, Cho K, Shin M-S et al. (2008) A novel electroporation method using a capillary and wire-type electrode. Biosens Bioelectron 23:1353–1360.